Jika suatu zat dicampurkan dengan
zat lain maka akan terjadi persebaran merata dari suatu zat ke zat lain yang
disebut SISTEM DISPERSI.
Zat yang didispersi disebut fase
terdispersi. Medium yang digunakan untuk mendispersi disebut medium
pendispersi
Berdasarkan ukuran pasrtikel, system dipersi terbagi
menjadi 3, antara lain :
- Larutan
- Koloid
- Suspensi
Gambar 1.
Contoh larutan, koloid, dan suspensi
1.
LARUTAN
Merupakan
sistem dispersi dengan ukuran partikel terdispersi sangat kecil. ( < 1 nm)
Umumnya merupakan
campuran homogeny. Karena ukuran partikelnya adalah molekul atau ion-ion,
sehingga sukar dipisahkan.
Partikel
pendispersi dan terdispersi tidak dapat dibedakan meskipun menggunakan
mikroskop ultra
Contoh :
larutan gula, larutan garam, larutan cuka, alkohol, bensin, dll
2. SUSPENSI
Merupakan
sistem dispersi dengan ukuran partikel terdispersi relatif besar dan tersebar
merata dalam medium pendispersinya. ( > 100 nm)
Pada
umumnya merupakan campuran heterogen. Partikel terdispersi dapat diamati menggunakan
mikroskop atau mata telanjang
Apabila
suspensi tidak diaduk terus-menerus, partikel terdispersi akan mengendap akibat
gaya grafitasi bumi
Suspensi
dapat dipisahkan dengan cara penyaringan.
Contoh :
campuran kopi dgn air, campuran air dengan pasir, campuran minyak dan air
3.
KOLOID
Suatu
campuran heterogen antara dua zat atau lebih di mana partikel-partikel zat yang
berukuran koloid (fase terdispersi) tersebar merata dalam zat lain (medium
pendispersi).
Pada
umumnya, Ukuran partikel terdispersi antara 1 nm – 100 nm. Oleh karena ukuran
partikelnya yang relative kecil, system koloid tidak dapat diamati secara
langsung, tapi dapat diamati menggunakan mikriskop ultra.
Contoh : sabun, susu,
jeli, mentega, dll
Tabel 1.
Perbandingan sifat larutan, koloid, dan suspensi
SIFAT-SIFAT KOLOID
Koloid
mempunyai sifat yang khas, antara lain sebagai berikut :
Efek Tyndall
Suatu system koloid dapat
dikenali dengan cara menghamburkan seberkas cahaya (sinar) kepada objek yang
akan dilihat.
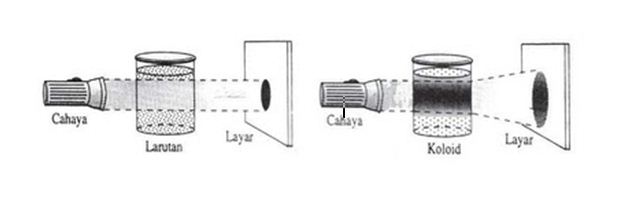
Gambar 2. Efek Tyndall
Bila dilihat tegak lurus dari
arah datangnya cahaya maka akan terlihat :
- Larutan
: cahaya akan diteruskan
- Koloid
: cahaya akan dihamburkan dan partikel terdispersinya tidak tampak
- Suspensi
: cahaya akan dihamburkan dan partikel terdispersinya dapat terlihat
• Contoh :
lampu mobil, lampu proyektor, dll
Gerak Brown
Partikel koloid bergerak terus-menerus dengan arah yang acak (tak beraturan) atau patah-patah (zig-zag). Gerakan partikel koloid ini disebut gerak Brown. Gerakannya Akan terlihat jelas menggunakan mikroskop
Gambar 3 Gerak Brown
Gerak Brown dengan lintasan lurus
dan arah yang acak karena terjadi saling benturan molekul molekul pendispersi pada
partikel terdispersi, sehingga partikel terdispersi akan terlontar. Peristiwa ini terjadi terus-menerus
karena ukuran partikel yang terdispersi relative besar dibandingkan medium
pendispersinya.
Gerak
Brown merupakan salah satu factor yang menstabilkan koloid. Karena partikelnya
yang bergerak terus-menerus, maka gaya grafitasi dapat diimbangi sehingga tidak
terjadi sedimentasi.
absorpsi
Adsorpsi
merupakan peristiwa penyerapan muatan oleh permukaan-permukaan partikel koloid. Hal ini
dapat terjadi karena adanya kemampuan pada partikel koloid untuk menarik
(ditempeli) oleh partikel-partikel kecil. Maka partikel koloid menjadi
bermuatan listrik. Kemampuan menarik inidisebabkan adanya tegangan permukaan
koloid yang cukup tinggi, sehingga partikel yang menempel akan cenderung
dipertahankan pada permukaannya.
Gambar 4. Peristiwa Adsorpsi
Bila partikel-partikel koloid
mengadsorbsi ion yang bermuatan positif pada permukaannya maka koloid akan
menjadi bermuatan positif, dan sebaliknya bila yang diadsorbsi ion negatif akan
menjadi bermuatan negative.
Muatan koloid merupakan salah
satu factor yang menstabilkan koloid. Karena partikel-partikel koloid bermuatan
sejenis maka akan saling tolak menolak sehingga terhindar dari pengelompokan
antar sesame partikel koloid itu.
Selain ion, partikel koloid dapat
menarik muatan dari listrik statis. Karena peristiwa adsorpsi, maka jika koloid
diletakan dalam medan listrik, partikelnya akan bergerak menuju kutub yang
muatannya berlawanan dengan muatan koloid itu. Peristiwa ini disebut elektroforesis.
Contoh dari peristiwa adsorpsi
dan elektroforesis seperti penjernih
air, penjernih air tebu, menyaringan debu pabrik, dll.
Koagulasi
Koagulasi yaitu peristiwa
penggumpalan partikel koloid. Peristiwa koagulasi dapat diakibatkan oleh peristiwa mekanis dan
peristiwa kimia.
·
Peristiwa mekanis : seperti pemanasan atau
pendinginan. Contoh darah merupakan butir-butir merah dalam plasma darah, jika
darah dipanaskan maka akan menggumpal.
·
Peristiwa kimia : seperti penambahan elektrolit
dalam koloid atau dengan sel elektroforesis
Gambar 5. Peristiwa Kogulasi
Contoh koagulasi dalam kehidupan sehari-hari,
misalnya Asap atau debu pabrik dapat
digumpalkan dengan alat koagulasi listrik Cottrel
Kestabilan Koloid
Kestabilan Koloid
Penambahan suatu zat ke dalam
sistem koloid dapat menstabilkan koloid, misalnya penambahan emulgator dan
koloid pelindung.
·
Emulgator
Emulgator
adalah zat yang ditambahkan dalam suatu emulsi (koloid cair dalam cair atau
cair dalam padat). Emulgator merupakan senyawa organik yang mengandung
kombinasi gugus polar dan non polar sehingga mampu mengikat zat polar (air) dan
zat non polar.
Contoh :
susu mengandung kasein yang berfungsi sebagai zat pengemulsi.
·
Koloid Pelindung
koloid
yang ditambahkan kedalam sistem koloid agar menjadi stabil.
Contoh :
penambahan gelatin pada pembuatan es krim.
Koloid Liofil dan Liofob
Koloid
yang memiliki medium pendispersi cair dibedakan atas koloid liofil dan koloid liofob. Koloid liofil lebih kental
daripada koloid liofob.
• Koloid
liofil : dimana partikel-partikel koloid yang dapat mengikat atau menarik
pelarutnya (cairannya)
Contoh: Agar Agar kanji, sagu,
• Koloid
Liofob : dimana sistim koloid yang partikel – partikelnya tidak dapat menarik
molckul-molekul pelarutnya.
Contoh : sol belerang sol emas, sistem koloid AgCl
JENIS-JENIS KOLOID
Terdapat tiga fase zat, yaitu padat, cair, dan gas. Dari ketiga fase zat ini dapat dibuat sembilan kombinasi campuran fase zat, akan tetapi yang dapat membentuk sistem koloid hanya delapan. Kombinasi campuran fase gas dan gas selalu menghasilkan larutan dimana campurannya menjadi homogen (satu fase) sehingga tidak dapat membentuk sistem koloid
Tabel 2.Jenis Koloid
1. Aerosol
Sistem koloid dari partikel padat
atau cair yang terdispersi dalam gas disebut aerosol. Jika zat yang
terdispersi berupa zat padat, disebut aerosol padat; jika zat yang
terdispersi berupa zat cair, disebut aerosol cair.
- Contoh aerosol padat: asap dan
debu dalamudara.
- Contoh aerosol : kabut dan
awan.
2.
Sol
Sistem koloid dari partikel padat
yang terdispersi dalam zat cair disebut sol.
Ada dua jenis sol, yaitu :
- Sol padat (padat dalam padat),
contoh : kaca berwarna
- Sol cair (padat dalam cair),
contoh : gel, agar-agar, dll.
3.
Emulsi
Sistem koloid dari zat cair yang
terdispersi dalam zat cair lain disebut emulsi. Syarat terjadinya emulsi ini adalah dua jenis zat cair
itu tidak saling melarutkan. Emulsi dapat digolongkan ke dalam 2 bagian, yaitu
:
- emulsi
minyak dalam air (M/A)
contoh : santan,
susu, kosmetik pembersih wajah (milk cleanser), dan lateks
- emulsi air dalam minyak (A/M)
contoh : mentega,
mayones, minyak bumi, dan minyak ikan.
4.
Buih
Sistem koloid dari gas yang
terdispersi dalam zat cair disebut Buih. Buih
dapat dibuat dengan mengalirkan suatu gas ke dalam zat cair yang
mengandung pembuih. Contoh : buih sabun pada pengolahan bijih logam, pada
alat pemadam kebakaran, dan lain-lain
PEMBUATAN
KOLOID
Koloid dapat dibuat
dengan dua acara, yaitu :
1. Dispersi
Adalah cara pembuatan sistem koloid dengan mengubah
partikel-partikel suspensi kasar menjadi partikel-partikel koloid.
- Dispersi langsung (mekanik) : dengan cara
digiling atau digerus
- Homogenisasi : dengan menggunakan mesin
homogenisasi
- Peptisasi : dengan bantuan zat pemeptisasi
(pemecah)
- Busur bredig : dengan menggunakan loncatan
bunga api listrik
2. Kondensasi
Kondensasi
: cara pembuatan sistem koloid dengan mengubah partikel-partikel koloid,
sehingga partikel-partikel zat terdispersi didalam larutan berupa ion, atom,
atau molekul diubah menjadi partikel yang lebih besar, yaitu koloid.
• Reaksi
hidrolisis : reaksi suatu zat dengan air
• Reaksi redoks : reaksi yang disertai perubahan bilangan oksidasi
• Pertukaran ion : membuat koloid dari zat yang sukar larut (endapan) yang dihasilkan dari reaksi kimia.
• Reaksi redoks : reaksi yang disertai perubahan bilangan oksidasi
• Pertukaran ion : membuat koloid dari zat yang sukar larut (endapan) yang dihasilkan dari reaksi kimia.
EVALUASI
1. Penghamburan berkas sinar di dalam sistem koloid disebut … .
A. gerak Brown D. elektroforesis
B. efek Tyndall E. osmose
C. koagulasi
A. gerak Brown D. elektroforesis
B. efek Tyndall E. osmose
C. koagulasi
2. Salah satu sifat penting dari dispersi koloid yang banyak
dimanfaatkan dalam bidang industri dan analisis biokimia adalah ....
A. prinsip elektroforesis D. homogenisasi
B. efek Tyndall E. peptisasi
C. gerak Brown
A. prinsip elektroforesis D. homogenisasi
B. efek Tyndall E. peptisasi
C. gerak Brown
3. Gerak Brown terjadi karena … .
A. gaya gravitasi
B. tolak-menolak antara partikel koloid yang bermuatan sama
C. tarik-menarik antara partikel koloid yang berbeda muatan
D. tumbukan antara partikel koloid
E. tumbukan molekul medium dengan partikel koloid
A. gaya gravitasi
B. tolak-menolak antara partikel koloid yang bermuatan sama
C. tarik-menarik antara partikel koloid yang berbeda muatan
D. tumbukan antara partikel koloid
E. tumbukan molekul medium dengan partikel koloid
4.
Partikel koloid
bermuatan listrik karena … .
A. adsorpsi ion-ion oleh partikel koloid D. pelepasan elektron oleh partikel koloid
B. absorpsi ion-ion oleh partikel koloid E. partikel koloid mengalami ionisasi
C. partikel koloid mengalami ionisasi
A. adsorpsi ion-ion oleh partikel koloid D. pelepasan elektron oleh partikel koloid
B. absorpsi ion-ion oleh partikel koloid E. partikel koloid mengalami ionisasi
C. partikel koloid mengalami ionisasi
5. Peristiwa koagulasi dapat ditemukan pada peristiwa … .
A. pembuatan agar-agar D. pembuatan air susu
B. terjadinya berkas sinar E. terjadinya delta di muara sungai
C. pembuatan cat
A. pembuatan agar-agar D. pembuatan air susu
B. terjadinya berkas sinar E. terjadinya delta di muara sungai
C. pembuatan cat
6. Zat-zat yang tergolong sol liofil adalah … .
A. belerang, agar-agar, dan mentega D. minyak tanah, asap, dan debu
B. batu apung, awan, dan sabun E. lem karet, lem kanji, dan busa sabun
C. susu, kaca, dan mutiara
A. belerang, agar-agar, dan mentega D. minyak tanah, asap, dan debu
B. batu apung, awan, dan sabun E. lem karet, lem kanji, dan busa sabun
C. susu, kaca, dan mutiara
7.
Gejala atau proses
yang paling tidak ada kaitan dengan sistem koloid adalah ... .
A. efek Tyndall D. emulsi
B. dialisis E. elektrolisis
C. koagulasi
A. efek Tyndall D. emulsi
B. dialisis E. elektrolisis
C. koagulasi
8. Di antara koloid berikut:
1) sol gelatin 4) sol belerang
2) sol logam 5) buih
3) agar-agar
Yang tergolong koloid hidrofil adalah ....
A. 1 dan 2 D. 2 dan 5
B. 1 dan 3 E. 2 dan 4
C. 1 dan 4
1) sol gelatin 4) sol belerang
2) sol logam 5) buih
3) agar-agar
Yang tergolong koloid hidrofil adalah ....
A. 1 dan 2 D. 2 dan 5
B. 1 dan 3 E. 2 dan 4
C. 1 dan 4
9. Dibandingkan dengan sol liofil, maka sol liofob … .
A. lebih stabil D. lebih mudah dikoagulasikan
B. lebih kental E. bersifat reversibel
C. memberi efek Tyndall yang kurang jelas
A. lebih stabil D. lebih mudah dikoagulasikan
B. lebih kental E. bersifat reversibel
C. memberi efek Tyndall yang kurang jelas
10. Contoh koloid hidrofob adalah ....
A. amilum dalam air D. lemak dalam air
B. protein dalam air E. agar-agar dalam air
C. karbon dalam air
A. amilum dalam air D. lemak dalam air
B. protein dalam air E. agar-agar dalam air
C. karbon dalam air
11. Tidak semua lampu
dapat digunakan untuk menerangi jalan pada saat berkabut. Hal ini
karena…..
A.
tidak
semua sinar lampu dapat dihamburkan oleh kabut
B.
hanya
sinar dari lampu dengan warna tertentu saja yang lebih dapat menembus kabut
akibat berbedanya efek tyndall untuk setiap sinar dengan panjang gelombang
berbeda
C.
setiap
sinar dari lampu dengan warna yang berbeda memiliki kesamaan dalam intensitas
cahaya yang dihamburkan oleh partikel koloid
D.
efek tyndall adalah sama untuk setiap
warna
E.
efek Tyndall tidak sama untuk setiap
sinar yang memiliki panjang gelombang berbeda sehingga sinar yang lebih banyak
dihamburkan lebih cocok digunakan untuk menerangi jalan pada saat berkabut
12. Gerak
Brown pada sistem koloid, akan membuat partikel koloid menjadi . . . .
A.
dapat
mengatasi pengaruh gravitasi sehingga partikel terdispersinya tidak memisahkan
diri dari medium pendispersinya
B.
dapat
mengatasi pengaruh gravitasi sehingga partikel terdispersinya memisahkan diri
dari medium pendispersinya
C.
tidak
dapat mengatasi pengaruh gravitasi sehingga sistem koloid mengalami pengendapan
(koagulasi)
D.
dapat bergerak ke segala arah sehingga
dapat menghamburkan cahaya
E.
dapat menyerap partikel-partikel padat
lain yang terlarut dalam suatu sistem koloid
13. Beberapa
aplikasi sistem koloid:
1. Pemutihan gula pasir
2. Penjernihan air
3. Pembentukan delta di muara sungai
4. Pewarnaan kain
5. Penyadapan karet
Yang
merupakan aplikasi dari sifat koloid adsorpsi adalah . . . .
A.
1, 3 dan 5 D. 2, 3 dan 4
B.
1, 2 dan 5 E. 3, 4 dan 5
C. 1,
2 dan 4
14. Partikel-partikel
koloid bersifat stabil karena memiliki muatan listrik sejenis. Namun jika
muatan listrik tersebut hilang, maka pertikel koloid tersebut akan mengalami .
. . .
A. dialisis D. ionisasi
B. adsorpsi E. koagulasi
C.
terasosiasi
- Suatu campuran heterogen yang terdiri dari zat terdispersi dan zat
pendispersi disebut
A.
larutan
sejati
B.
suspensi
kasar
C.
koloid
D.
dispersi
kasar
E.
dispersi
molekular
- Perbedaan antara sistem koloid dengan suspensi adalah…..
A. koloid
dapat disaring menggunakan kertas saring, suspensi tidak.
B.
ukuran
partikel koloid berkisar antara 10-9 cm – 10-7 cm,
sedangkan suspensi berkisar antara 10-7 cm – 10-5 cm.
C.
jumlah
fase koloid ada dua, sedangkan suspensi hanya satu.
D.
koloid umumnya bersifat stabil,
sedangkan suspensi tidak.
E.
koloid meneruskan sinar jika disenter,
suspensi membiaskannya.
- Diketahui suatu campuran
memiliki sifat-sifat sebagai berikut :
-
Jumlah fase : 2
-
Distribusi partikel :
heterogen
-
Penyaringan : dapat disaring
Campuran
tersebut tergolong….
A.
larutan D. koloid
B.
emulsi E. suspensi
C.
sol
18. Berikut
ini yang merupakan contoh sistem koloid adalah…..
A. campuran gula dengan air D. campuran garam dengan air
B. campuran susu
dengan air E. campuran tanah dengan air
C. campuran pasir dengan air
- Berdasarkan fasa terdispersi
dan medium pendispersinya, maka koloid dapat dikelompokkan menjadi…..
A. sol, emulsi, dan larutan D.
sol, emulsi, dan buih
B. sol, emulsi, dan dispersi kasar E. sol, emulsi, dan
bubuk
C. sol, emulsi, dan dispersi molekular
20. Sistem koloid yang tersusun dari fase terdispersi gas dan
fase pendispersi padat disebut . . . .
A.
emulsi
padat D. buih cair
B.
emulsi gas E. buih padat
C.
sol gas
Essay !
Berikan contoh lain (selain yang sudah dicontohkan) yang ada
dilingkungan sekitar yang termasuk dalam :
a.
Larutan
b.
Suspense
c.
Koloid
















0 komentar: